I VACCINI NON CADONO DAL CIELO: Lo scatto in avanti del Jenner Institute
Lo sviluppo di un vaccino efficace contro il virus
SARS-CoV-2 è comunemente considerato l’unico evento in grado di mettere
fine alla pandemia di COVID-19 in tempi relativamente brevi. La corsa al
vaccino è in pieno svolgimento, con la registrazione presso le autorità
sanitarie di almeno 70 diversi progetti. Finora la maggior parte degli esperti ha
pensato che, se tutto andrà nel migliore dei modi, per avere un vaccino dovremo
aspettare almeno 12-18 mesi.
Produrre un vaccino contro un nuovo virus è un processo lungo, per niente scontato. Pensate solo ad HIV: 40 anni dopo l’esplosione dei primi casi, il vaccino non esiste ancora!
Eppure, un articolo del New York Times ha annunciato che il Jenner Institute dell’Università di Oxford sta per iniziare uno studio di fase II e III per un vaccino molto promettente. Lo studio coinvolgerà complessivamente circa 6000 volontari, ed è stato pensato non solo per valutare la sicurezza del vaccino (fase I), ma anche per valutarne l’efficacia. Se tutto andasse bene, il vaccino potrebbe essere rilasciato prima della fine dell’estate, con mesi di anticipo sulle previsioni più ottimistiche. Da allora, potrebbe essere prodotto su scala industriale da molte ditte diverse, perché il Jenner Institute è un’organizzazione no-profit, intenzionata a concedere molte licenze non esclusive per la produzione del virus.
Sembra quasi un miracolo, ma come è possibile? Come ha fatto il team inglese ad arrivare così rapidamente alla sperimentazione sull’uomo?
La risposta è semplice e dimostra ancora una volta che nella scienza nessun risultato applicativo viene raggiunto facilmente, senza anni di duro lavoro impiegato in ricerche ‘di base’. Il team di Oxford ha fatto così in fretta perché era ad un punto molto avanzato nello sviluppo di un vaccino contro un altro Coronavirus, quello responsabile della MERS. Per essere ancora più precisi, la storia di questa piattaforma vaccinale è ancora più lunga, perché parte da un tentativo (finora non molto riuscito) di produrre un vaccino contro la malaria.
Voglio raccontarvi a grandi linee i passaggi fondamentali che hanno portato agli ultimi sviluppi, spiegandovi anche alcuni dettagli tecnici, per farvi capire che procedure dal nome inquietante come ingegnerizzazione di genomi virali nei batteri, produzione di virus ricombinanti e sperimentazione animale controllata sono assolutamente essenziali per ottenere risultati significativi sull’uomo, senza fargli correre pericoli irragionevoli.
Il papà di questa piattaforma vaccinale è Adrian Hill, Direttore del Jenner Institute. Per produrre un vaccino contro la malaria, il suo team ha iniziato molti fa anni a ingegnerizzare gli Adenovirus. Questi virus sono molto diversi dai Coronavirus perché hanno un genoma costituito da DNA, invece che RNA, e codificano per proteine totalmente diverse. Gli Adenovirus non sono molto pericolosi: in genere provocano un banale raffreddore. Inizialmente sono stati studiati come possibili ‘corrieri’ (o vettori), per curare le malattie genetiche.
L’idea di base sottostante il loro utilizzo in medicina non è tanto complicata: si prende il DNA dell’Adenovirus, si eliminano tre geni, essenziali perché il virus si possa riprodurre, si mette al loro posto la sequenza di un gene che si vuole trasferire nelle cellule. Nella terapia genica, si tratta della versione normale di un gene che manca alle cellule del paziente.
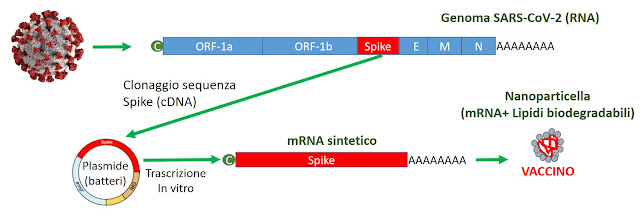
Nel caso dei vaccini, si introduce nel genoma virale la sequenza che codifica la proteina di superficie del virus si vuole combattere (la proteina Spike, nel nostro caso). Il genoma artificiale viene impacchettato in particelle adenovirali e queste vengono usate per infettare cellule normali del soggetto da vaccinare, mediante un’iniezione. L’infezione non è pericolosa, perchè il virus non si può replicare. Le cellule infettate producono la Spike protein, insieme ad alcune proteine dell’Adenovirus. Il sistema immunitario riconosce queste strane cellule, si attiva contro di esse e, se tutto va per il verso giusto, produce anticorpi in grado di neutralizzare le proteine Spike. La presenza di questi anticorpi e di linfociti capaci di riconoscere le cellule infettate protegge l’organismo, se dovesse successivamente infettarsi con il Coronavirus vero. Uno schema un po' semplificato di questo approccio è riportato nella figura.
La produzione di questi virus ricombinanti può fare molta
paura, ma in realtà si tratta di un sistema molto sicuro, come hanno dimostrato
decenni di sperimentazione condotta sugli animali e sull’uomo. Le particelle di
Adenovirus ricombinante possono infettare le cellule umane, ma dopo che lo
hanno fatto non si possono propagare, a causa della eliminazione dei geni E1A,
E1B ed E3. Inoltre, se per errore le preparazioni di virus contenessero
particelle con un genoma normale, la malattia prodotta sarebbe molto lieve.
Il motivo che rende questi vettori poco adatti alla terapia genica, ma molto adatti alla produzione di vaccini, è la forte reazione del sistema immunitario contro le proteine dell’Adenovirus. Nella terapia genica, lo sviluppo di anticorpi contro queste proteine impedisce di effettuare trattamenti multipli. Invece, nel caso dei vaccini, la risposta contro le proteine di Adenovirus rappresenta un ‘bonus’ formidabile, perché aiuta il sistema immunitario a riconoscere meglio la proteina Spike. Questa azione adiuvante è importantissima, perché la proteina Spike può passare inosservata al sistema immunitario a causa delle sue ‘caratteristiche stealth’.
Il progetto del Jenner Institute ha alcune caratteristiche che lo distinguono dai progetti concorrenti, in particolare:
1. L’Adenovirus usato come vettore non è umano, ma di scimmia (ChAdOx1). Questo riduce moltissimo la possibilità che i soggetti iniettati col vaccino abbiano già anticorpi contro le proteine adenovirali, evento che impedirebbe l’infezione delle cellule, e quindi la produzione delle proteine Spike.
2. Tutti gli elementi della piattaforma sono già stati testati nell’uomo negli ultimi 20 anni, in circa 70 trial clinici di possibili vaccini contro la malaria, che ne hanno dimostrato la grande sicurezza.
3. All’interno del Jenner Institute, il gruppo della Prof.ssa Sarah Gilbert stava usando da molto tempo la piattaforma ChAdOx1 per produrre un vaccino contro il Cronavirus della MERS, molto simile a quello responsabile di COVID-19. In particolare:
5. In considerazione di tutti i dati di sicurezza già disponibili sulla piattaforma ChAdOx1, ottenuti su modelli sperimentali animali e sull’uomo, per il gruppo del Jenner Institute è stato molto facile convincere le autorità regolatorie inglesi che non fosse molto rischioso sperimentare il vaccino candidato in uno studio di fase I sull’uomo, partito la scorsa settimana con l’iniezione su 1100 volontari.
6. In parallelo, è già stato condotto uno studio su 6 macachi. Queste scimmiette rappresentano per ora l’unico modello sperimentale per COVID-19 sufficientemente vicino all’uomo. Anche se i risultati non sono stati ancora pubblicati, dalle anticipazioni del NYT pare che i sei macachi, iniettati con un’unica dose di vaccino ChAdOx1-nCoV-19, abbiano sviluppato una buona risposta anticorpale. Inoltre sembrerebbero ancora in perfetta salute, 28 giorni dopo essere stati esposte a una dose massiccia del virus vero, che provoca una sindrome respiratoria meno grave di quella umana nelle scimmie non vaccinate.
7. La sperimentazione su altri 5000 volontari umani partirà la prossima settimana, in un momento in cui in Inghilterra ci sono ancora molti casi. Questo dovrebbe permettere di capire in maniera relativamente rapida se il virus funziona veramente, perché è ragionevole aspettarsi qualche decina di contagiati tra i volontari non iniettati col vaccino. Appena la statistica dimostrasse l’efficacia del vaccino oltre ogni ragionevole dubbio statistico, si procederà ad iniettarlo anche i volontari che hanno ricevuto il placebo.
In considerazione dell’enorme mole di lavoro preliminare, il vaccino del Jenner Institute sembra essere più che in pole position nella corsa per il primo vaccino efficace. Le speranze sono alte, potendo fondarsi su una base scientifica ed etica di tutto rispetto. Facciamo tutti il tifo per la riuscita di questo progetto! Anche nella malaugurata ipotesi di un fallimento, i risultati scientifici di questo trial ci permetteranno sicuramente di acquisire informazioni fondamentali, preziosissime per tutti gli altri progetti in corsa!!
Produrre un vaccino contro un nuovo virus è un processo lungo, per niente scontato. Pensate solo ad HIV: 40 anni dopo l’esplosione dei primi casi, il vaccino non esiste ancora!
Eppure, un articolo del New York Times ha annunciato che il Jenner Institute dell’Università di Oxford sta per iniziare uno studio di fase II e III per un vaccino molto promettente. Lo studio coinvolgerà complessivamente circa 6000 volontari, ed è stato pensato non solo per valutare la sicurezza del vaccino (fase I), ma anche per valutarne l’efficacia. Se tutto andasse bene, il vaccino potrebbe essere rilasciato prima della fine dell’estate, con mesi di anticipo sulle previsioni più ottimistiche. Da allora, potrebbe essere prodotto su scala industriale da molte ditte diverse, perché il Jenner Institute è un’organizzazione no-profit, intenzionata a concedere molte licenze non esclusive per la produzione del virus.
Sembra quasi un miracolo, ma come è possibile? Come ha fatto il team inglese ad arrivare così rapidamente alla sperimentazione sull’uomo?
La risposta è semplice e dimostra ancora una volta che nella scienza nessun risultato applicativo viene raggiunto facilmente, senza anni di duro lavoro impiegato in ricerche ‘di base’. Il team di Oxford ha fatto così in fretta perché era ad un punto molto avanzato nello sviluppo di un vaccino contro un altro Coronavirus, quello responsabile della MERS. Per essere ancora più precisi, la storia di questa piattaforma vaccinale è ancora più lunga, perché parte da un tentativo (finora non molto riuscito) di produrre un vaccino contro la malaria.
Voglio raccontarvi a grandi linee i passaggi fondamentali che hanno portato agli ultimi sviluppi, spiegandovi anche alcuni dettagli tecnici, per farvi capire che procedure dal nome inquietante come ingegnerizzazione di genomi virali nei batteri, produzione di virus ricombinanti e sperimentazione animale controllata sono assolutamente essenziali per ottenere risultati significativi sull’uomo, senza fargli correre pericoli irragionevoli.
Il papà di questa piattaforma vaccinale è Adrian Hill, Direttore del Jenner Institute. Per produrre un vaccino contro la malaria, il suo team ha iniziato molti fa anni a ingegnerizzare gli Adenovirus. Questi virus sono molto diversi dai Coronavirus perché hanno un genoma costituito da DNA, invece che RNA, e codificano per proteine totalmente diverse. Gli Adenovirus non sono molto pericolosi: in genere provocano un banale raffreddore. Inizialmente sono stati studiati come possibili ‘corrieri’ (o vettori), per curare le malattie genetiche.
L’idea di base sottostante il loro utilizzo in medicina non è tanto complicata: si prende il DNA dell’Adenovirus, si eliminano tre geni, essenziali perché il virus si possa riprodurre, si mette al loro posto la sequenza di un gene che si vuole trasferire nelle cellule. Nella terapia genica, si tratta della versione normale di un gene che manca alle cellule del paziente.
Nel caso dei vaccini, si introduce nel genoma virale la sequenza che codifica la proteina di superficie del virus si vuole combattere (la proteina Spike, nel nostro caso). Il genoma artificiale viene impacchettato in particelle adenovirali e queste vengono usate per infettare cellule normali del soggetto da vaccinare, mediante un’iniezione. L’infezione non è pericolosa, perchè il virus non si può replicare. Le cellule infettate producono la Spike protein, insieme ad alcune proteine dell’Adenovirus. Il sistema immunitario riconosce queste strane cellule, si attiva contro di esse e, se tutto va per il verso giusto, produce anticorpi in grado di neutralizzare le proteine Spike. La presenza di questi anticorpi e di linfociti capaci di riconoscere le cellule infettate protegge l’organismo, se dovesse successivamente infettarsi con il Coronavirus vero. Uno schema un po' semplificato di questo approccio è riportato nella figura.
Il motivo che rende questi vettori poco adatti alla terapia genica, ma molto adatti alla produzione di vaccini, è la forte reazione del sistema immunitario contro le proteine dell’Adenovirus. Nella terapia genica, lo sviluppo di anticorpi contro queste proteine impedisce di effettuare trattamenti multipli. Invece, nel caso dei vaccini, la risposta contro le proteine di Adenovirus rappresenta un ‘bonus’ formidabile, perché aiuta il sistema immunitario a riconoscere meglio la proteina Spike. Questa azione adiuvante è importantissima, perché la proteina Spike può passare inosservata al sistema immunitario a causa delle sue ‘caratteristiche stealth’.
Il progetto del Jenner Institute ha alcune caratteristiche che lo distinguono dai progetti concorrenti, in particolare:
1. L’Adenovirus usato come vettore non è umano, ma di scimmia (ChAdOx1). Questo riduce moltissimo la possibilità che i soggetti iniettati col vaccino abbiano già anticorpi contro le proteine adenovirali, evento che impedirebbe l’infezione delle cellule, e quindi la produzione delle proteine Spike.
2. Tutti gli elementi della piattaforma sono già stati testati nell’uomo negli ultimi 20 anni, in circa 70 trial clinici di possibili vaccini contro la malaria, che ne hanno dimostrato la grande sicurezza.
3. All’interno del Jenner Institute, il gruppo della Prof.ssa Sarah Gilbert stava usando da molto tempo la piattaforma ChAdOx1 per produrre un vaccino contro il Cronavirus della MERS, molto simile a quello responsabile di COVID-19. In particolare:
- nel 2017 ha dimostrato che il vaccino ChAdOx1-MERS è sicuro ed efficace nei topi;
- nel 2019 ha dimostrato che il vaccino ChAdOx1-MERS è efficace nei dromedari, che rappresentano il veicolo della MERS;
- pochi gironi fa ha pubblicato i risultati di uno studio di fase I, che dimostra la sicurezza e l’immunogenicità del vaccino ChAdOx1-MERS nell’uomo.
5. In considerazione di tutti i dati di sicurezza già disponibili sulla piattaforma ChAdOx1, ottenuti su modelli sperimentali animali e sull’uomo, per il gruppo del Jenner Institute è stato molto facile convincere le autorità regolatorie inglesi che non fosse molto rischioso sperimentare il vaccino candidato in uno studio di fase I sull’uomo, partito la scorsa settimana con l’iniezione su 1100 volontari.
6. In parallelo, è già stato condotto uno studio su 6 macachi. Queste scimmiette rappresentano per ora l’unico modello sperimentale per COVID-19 sufficientemente vicino all’uomo. Anche se i risultati non sono stati ancora pubblicati, dalle anticipazioni del NYT pare che i sei macachi, iniettati con un’unica dose di vaccino ChAdOx1-nCoV-19, abbiano sviluppato una buona risposta anticorpale. Inoltre sembrerebbero ancora in perfetta salute, 28 giorni dopo essere stati esposte a una dose massiccia del virus vero, che provoca una sindrome respiratoria meno grave di quella umana nelle scimmie non vaccinate.
7. La sperimentazione su altri 5000 volontari umani partirà la prossima settimana, in un momento in cui in Inghilterra ci sono ancora molti casi. Questo dovrebbe permettere di capire in maniera relativamente rapida se il virus funziona veramente, perché è ragionevole aspettarsi qualche decina di contagiati tra i volontari non iniettati col vaccino. Appena la statistica dimostrasse l’efficacia del vaccino oltre ogni ragionevole dubbio statistico, si procederà ad iniettarlo anche i volontari che hanno ricevuto il placebo.
In considerazione dell’enorme mole di lavoro preliminare, il vaccino del Jenner Institute sembra essere più che in pole position nella corsa per il primo vaccino efficace. Le speranze sono alte, potendo fondarsi su una base scientifica ed etica di tutto rispetto. Facciamo tutti il tifo per la riuscita di questo progetto! Anche nella malaugurata ipotesi di un fallimento, i risultati scientifici di questo trial ci permetteranno sicuramente di acquisire informazioni fondamentali, preziosissime per tutti gli altri progetti in corsa!!



Commenti
Posta un commento